漫長的新藥開發與藥品專利制度簡介
文 / 鍾富澄
行政院於2009年提出『生技起飛鑽石行動方案』的發展策略,已促成設立食品藥物管理局 (FDA),著手建置與國際銜接的法規環境,加入PIC/S GMP國際品質組織,強化國內生技醫藥研發單位。我國政府對生技醫藥之研發投資不小,尤其國科會、經濟部、衛生署都有補助藥物研發計畫之經費,又因世界人口老化快速因此新藥研發是我國生物科技產業未來的發展重點!
新藥的開發
一個新藥的誕生,由實驗室到產品上市,研發時程長達10-15 年,且後續藥品上市後還需要產品行銷約2-3年,所耗資金達180~250 億台幣相當龐大。由於藥物的研發相當複雜,幾乎所有的新藥都會跑一個既定的流程與規範新藥的定義,依據藥事法第七條乃新成份、新療效複方或新使用途徑的藥品。
新藥上市許可的審核流程,主要可分為:
第一階段: 藥品臨床試驗申請階段
填寫藥品臨床試驗收件通知表並備妥資料藥物的組成與來源、製造方法、臨床試驗計畫書與相關執行者..等,審查時間約在30天至幾個月之間若沒有問題即可開始進行臨床試驗。
第二階段:臨床試驗
試驗中新藥必須通過臨床試驗前三期 (Phase I ~ Phase III),才會被允許提出新藥上市許可申請NDA(New Drug Application)。
Phase I clinical trial:此階段主要為確認新藥的安全性,決定安全劑量的範圍以及評估整體的安全性。實驗對象是健康的一般人,測試時間約1-2年。
Phase II clinical trial:這階段以小規模罹患疾病的病人為實驗對象以雙盲對照試驗測試療效病人在這個試驗中不知道自己是不是吃新藥(實驗時會將新藥和安慰劑做的一模一樣);參與實驗的執行醫師也不知道給病人吃的是新藥和安慰劑。只有這個實驗的主持人知道哪一位病人是使用新藥,那一位病人使用的是安慰劑。這樣可以讓實驗更精確,避開藥物實驗兩個最頭痛的問題:觀察者期望效應和安慰劑效應。
Phase III clinical trial:一般認為第三期起始於主要目的為顯示或確認治療效益之試驗。第三期試驗主要目的,為確認於第二期中所得藥品用於目標適應症及受試驗者是安全及有效的 初步證據。這些試驗的目的在提供核准藥品上市之適當依據。第三期試驗可更進一步地探索劑量-反應關係,或探討將此藥品使用於更多族群、或用於疾病之不同 階段、或與不同藥品合併使用。對需長期給藥的藥品而言,雖然第二期可進行長期給藥之臨床試驗,但此類臨床試驗通常於第三期進行,第三期所執行之試驗 提供完整資訊,以支持藥品的適當使用說明。 如果能成功完成第三期,那就可以向FDA提出新藥上市申請。但在美國,要取得新藥申請NDA,一般需要兩個獨立的第三期臨床試驗研究,才可能被批准通過。
第三階段:銷售後試驗追蹤
Phase IV clinical trial:第四期稱之為銷售後之試驗 ,此階段是藥品上市後的追蹤,監測該藥物是否有先前幾個階段沒發現的副作用或是不良反應等情況,試驗設計較為簡單,但是需要大量的病人進行長時間的觀察。
藥品專利制度:
1.藥品專利依靠的法源即是『專利法』,新藥藥品開發時間漫長需時10-15年的時間,通常藥品通過NDA專利保護時間已經過了大半,專利權到期後,其他藥廠將可以依循法規推出成分相同的藥品稱之『學名藥』瓜分市場,目前全球製藥業正面臨到大批藥品專利到期約2013-2020年將達到高峰。
發明專利的保護期限為自申請日起20年,且專利法另外設有專利權的延長制度,用來補償因醫藥品審查過程所耗費的專利權保護時間(核准延長期間,不能超過取得許可證所需時間) ,此延長辦法是依據專利法53條規定: 醫藥品、農藥品或其製造方法發明專利權之實施,依其他法律規定,應取得許可證者,其於專利案公告後取得時,專利權人得以第一次許可證申請延長專利權期間,並以一次為限,且該許可證僅得據以申請延長專利權期間一次。
前項核准延長之期間,不得超過為向中央目的事業主管機關取得許可證而無法實施發明之期間;取得許可證期間超過五年者,其延長期間仍以五年為限。
2.得延長之專利權期間:
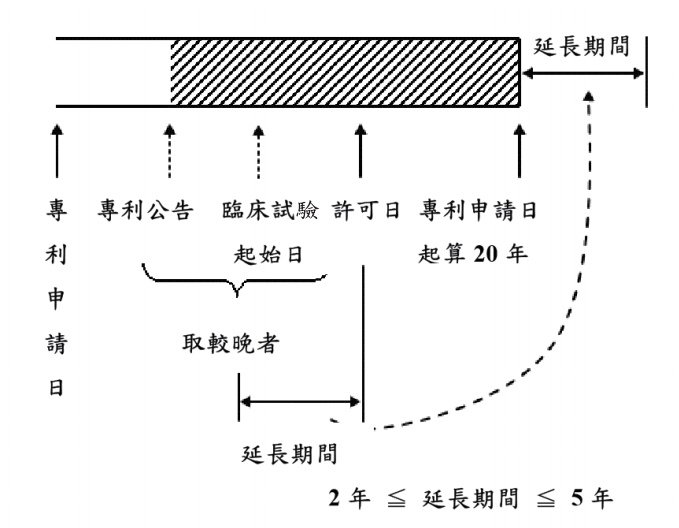
若醫藥品專利權人為取得實施許可,自其專利公告日起算,有至少二年未能實施其發明時,得針對該為取得實施許可而於專利公告後所花費之時間申請專利權期間延長,所能取得之延長 期間最長為五年。所謂「未能實施其發明」之期間,根據前開「專 利權期間延長」審查基準之規定,係包括於專利核准公告後,為取得許可而於臨床試驗及查驗登記所花費的時間,且須扣除申請人未適當實施之時間。其中,臨床試驗之起算日為主管機關所認可之臨床試驗開始日,該期日若早於發明專利核准公告日,則延長時間之起算日為專利核准公告日。以下圖表示:
總結
台灣新藥公司因近年來各國法規日益嚴格,使得新藥在開發上面難度越來越高,歐美大廠各國專利競爭也日趨激烈,既然藥品開發是漫長的那更應該注重專利之佈局,全球專利藥品到期潮即將來臨,若能加速新藥的開發與專利的佈局也將能為未來的新藥市場搶得先機。
財團法人醫藥品查驗中心官網 / 股感知識庫 科學月刊 / 智慧財產權月刊 115 期